CLINUVEL Kommuniqué II
Liebe Aktionäre, Freunde
Wir begrüßen viele neue Aktionäre, insbesondere die große Anzahl deutschsprachiger Investoren, die die Geschichte von CLINUVEL in den letzten drei Monaten entdeckt haben. Natürlich werden wir unsere News Communiqués weiterhin in deutscher Sprache veröffentlichen. Für neue Leser sind die News Communiqués ein Kontinuum von Aktualisierungen zu spezifischen und relevanten regulatorischen, klinischen, finanziellen und Marktthemen. Einige Unternehmensthemen bleiben vertraulich, um das Unternehmen vor Wettbewerbsdruck zu schützen. In einem neuartigen Format wird das Strategic Update II, das nach Ostern veröffentlicht werden soll, und eine Fortsetzung von Strategic Update I, 29. Oktober 2020 ist, systematisch die Fortschritte des Unternehmens pro Geschäftsbereich, sein Forschungs und Entwicklungs- Programm und andere relevante Themen erörtern.
Seit der Veröffentlichung von News Communiqué I am 25. Januar halten wir inne und blicken auf ein ereignisreiches erstes Quartal zurück, das von der Einführung von vier zugelassenen COVID-Impfungen dominiert wird. Im März beschleunigte die Europäische Arzneimittel-Agentur (EMA) die Zulassung eines vierten Antivirenprogramms von Janssen, das eine einmalige Impfung ermöglichte. Ohne die Präferenz für eines der vier verfügbaren Mittel auszudrücken, haben israelische Daten gezeigt, dass das Pfizer-Mittel zu 97% wirksam zu sein scheint.
Im Februar wurden Schlagzeilen gemacht, als wir miterlebten, wie Gamestop, eine Aktie, die von syndizierten Hedge-Fonds kurz angegriffen wurde, die Aufmerksamkeit der Privatanleger spekulativ auf sich gezogen hatte, als sie sich gegen die drei Hedge-Fonds erholten, die die Aktie geshortet hatten. Die Kaufunterstützung auf dem Markt wurde über Reddit koordiniert. Als sich der Aktienkurs Ende Januar katapultierte und das Unternehmen von einer Bewertung von 3 Mrd. USD auf eine Bewertung von 22 Mrd. USD anstieg, stellte sich die Frage nach der Rolle des Clearance-Hauses Robinhood und seinen Verbindungen zu seinen Kunden Melvin Capital und Point72. Als sich der Wind gelegt hatte, wurde die fundamentale Bewertung von Gamestop, einem Einzelhandelsunternehmen für Onlinespiele, zum Schwerpunkt.
ch betrachte das Reddit-Phänomen als eines, das die Gesamtmacht der US-Einzelhandelsaktionäre veranschaulicht, die Einfluss ausüben, wenn es darauf ankommt. Ich glaube, wir werden mehr Raserei bei Wertpapieren erleben, da sich die Welt weiterhin schneller verbindet und den Nachrichtenfluss von Unternehmen verbreitet, sobald er entsteht.
m März erfuhren wir, wie sich US-Banken und -Märkte vom Ausfall von Archegos Capital Management erholten. Die größeren US-Investmentbanken hatten es dem Family Office ermöglicht, über Swap-Kontrakte ein Engagement in volatilen Aktien in Milliardenhöhe zu übernehmen, bis Margin Calls durch einen Einbruch der Märkte ausgelöst wurden. Dies zeigt, wie die Wette auf ein schief gelaufenes Wertpapier, in diesem Fall ViacomCBS-Aktien, sofort zu einer internationalen Proportionskaskade führen kann. Da zwei der größten Investmentbanken auf der Straße an einem Tag Positionen in US-amerikanischer und chinesischer Sprache in Höhe von bis zu 19 Milliarden US-Dollar liquidiert hatten, mussten viele andere Portfoliomanager mit einem Blockverkauf zu ermäßigten Preisen reagieren. Wenn man bedenkt, dass dieses Ereignis kaum einen Monat nach dem Aufdecken des Engagements von Greensill in Höhe von 3 Milliarden US-Dollar in der Credit Suisse stattgefunden hat, können die Anleger erraten, wie sich dieses Ereignis hätte auflösen können. Archegos erinnert an das LTCM-Debakel des Hedgefonds von 1998, als die US-Regierung keine andere Wahl hatte, als den Fonds zu retten. Im Kern liegen gehebelte Bilanzen und uneingeschränkte Kreditvergabe durch Banken den Kaskaden zugrunde, die sich entfalten, wenn Margin Calls und Verstöße gegen Covenants nicht mehr vermeidbar sind. Der unerbittliche Glaube an das Vermögen bei gehebelten Wetten auf den Märkten wiederholt sich immer wieder. Portfoliomanager gleichen ihre Bestände schließlich unabhängig von der Unternehmensleistung neu aus, und die Aktionäre zahlen den Preis.
Beim Scannen der Makroentwicklungen der Welt überdenken wir ständig den Kurs von CLINUVEL, und derzeit sehe ich die langfristigen Auswirkungen der zunehmenden Spannungen zwischen China und den USA, Europa und Australien auf die westlichen Volkswirtschaften düster. Die Diskussionen in Anchorage lassen wenig Aufschluss über die Richtung dieser gegensätzlichen politischen Ansichten zum Klimawandel und zu den Handelsbeziehungen. Während wir zwei Haltungslager gesehen haben, sehe ich kurzfristig wenig Veränderung voraus. Die ökopolitischen Spannungen werden weiter angeheizt, da Moskau seinen Botschafter in den USA, wie die bilateralen Entscheidungen genannt werden, zurückgerufen hat – als “Spirale in Richtung einer Sackgasse”.
Für diejenigen, die uns regelmäßig folgen, teile ich, dass im Rahmen der Beratungen im Verwaltungsrat von CLINUVEL makroökonomische Fragen wie das Handelsungleichgewicht zwischen China und den USA und Europa sowie die anhaltenden Spannungen im asiatisch-pazifischen Raum und im Südchinesischen Meer unsere Aufmerksamkeit auf sich ziehen. Globale Ereignisse prägen unser Denken über CLINUVEL und die Navigation eines börsennotierten Unternehmens durch viele Hindernisse. Ich glaube, von uns wird erwartet, dass wir die kurzfristigen Auswirkungen der Makroverschiebungen, die wir beobachten, und insbesondere die möglichen Auswirkungen auf unser Geschäft und unsere Lieferketten berücksichtigen.
Angebot und Verteilung im Zusammenhang mit der Gesundheitsversorgung werfen Fragen auf, da eine gerechte Verteilung der Ressourcen pro Land mittlerweile zu einem vorherrschenden Thema geworden ist und Pharma-Deals mit Regierungen bestimmte Nationen benachteiligen. Die jüngsten nationalen verbalen Auseinandersetzungen in Europa über die Freisetzung von Impfstoffen und Kämpfe zum Schutz des geistigen Eigentums auf der Suche nach einem globalen Gemeinwohl sind kein gutes Zeichen für diejenigen, die an die Globalisierung als treibende wirtschaftliche Kraft glauben. Ich denke, wir treten schnell in eine „Entspannung“ ein, in der die Selbstversorgung unsere politischen und wirtschaftlichen Entscheidungen dominieren wird.
Wenn man in die USA wechselt, kann man nicht anders, als die Gesetzesvorlage des Kongresses für ein Konjunkturpaket in Höhe von 1,9 Billionen US-Dollar zu begrüßen, das am 11. März, dem sechsten COVID Relief Bill, verabschiedet wurde. Dieser historische Rekord zur Ankurbelung der Wirtschaft muss in den Kontext der gesamtwirtschaftlichen Anreize seit Anfang 2020 gestellt werden, die sich auf mehr als 5 Billionen US-Dollar beliefen und vor 18 Monaten unvorstellbar waren.
Seit der Amtseinführung von Präsident Biden gibt es keine Nachrichten aus Capitol Hill über seine Haltung zur Preisgestaltung für Arzneimittel. Die neueste Nachricht ist, dass die Biden-Regierung Pläne zur Reform des Medicare-Teils D und der aktuellen Rabatte für Medicaid Managed Care bis 2023 zurückgestellt hat. Wir verweisen auf das Nachrichten-Kommuniqué vom Februar 2019 ueber die Diskussion des günstigsten Nationen-Modell, das von der Trump-Administration umgesetzt wurde; dieses hat nun erneut Aufmerksamkeit von Vizepräsidentin Kamala Harris erhalten.
Gegenwärtig zielt die Diskussion in demokratischen Ecken der Verwaltung darauf ab, Wege zu finden, die Listenpreise zu begrenzen und gleichzeitig dem Patienten zu helfen. Die Preisgestaltung für Arzneimittel ist jedoch nur ein kleiner Teil des wahrgenommenen Problems. Die tieferen Probleme liegen beim Versicherungssystem selbst. US-amerikanische Patienten ohne Versicherung und diejenigen, die Pläne mit hohem Selbstbehalt und Mitversicherung abgeschlossen haben, benötigen die dringendste politische Hilfe. Die Senkung der Arzneimittelpreise hat möglicherweise nur einen geringen Einfluss auf die Auslagenkosten, je nachdem, wie sich die Versicherungsunternehmen auf mögliche künftige Vereinbarungen zur Kostenteilung einstellen. Derzeit sind wir nicht optimistisch, dass das US-amerikanische System zur Erstattung von Arzneimitteln überarbeitet werden kann, da zu viele Akteure und Vermittler bei verschreibungspflichtigen Arzneimitteln eine Rolle spielen.
Im Fall von CLINUVEL geben das direkte Vertriebsmodell an Krankenhäuser, die mangelnde Verfügbarkeit in US-Apothekenketten und die genau definierte Patientenpopulation, für die eine vorherige Genehmigung erforderlich ist, den Versicherern viel Kontrolle über den Arzneimittelpreis und die Patienten, die eine Behandlung erhalten.
Richten wir die Aufmerksamkeit auf Anderes; wie in früheren Nachrichtenmitteilungen (siehe Juli und September 2020) erörtert, konzentrieren wir uns weiterhin stark auf Zinssätze und Inflation. Mit Spannung warten wir auf das nächste Quartal, um zu beobachten, wie die Märkte auf die schleichende Inflation, die negativen US-Renditen und die rekordhohen Bewertungen von Technologieaktien und bestimmten Marktsektoren reagieren. Dennoch scheint es eine weit verbreitete Überzeugung zu geben, dass die wirtschaftliche Erholung schneller sein koennte als im Dezember 2020 prognostiziert; wobei ein Wachstum bei Wertaktien, wertorientierten Anlagen und Immobilien erwartet wird, aber eine Abschwaechung der festverzinslichen Wertpapiere.
Mit Besorgnis verfolgen wir die wirtschaftliche Debatte über die Möglichkeit von Zinserhöhungen als einen unwahrscheinlichen Faktor, der das Wirtschaftswachstum in den nächsten Jahren bremst, wobei der Wert von Bargeld weiterhin ein heißer Streitpunkt bleibt. Da CLINUVEL wächst und gezwungen ist, Investitionsentscheidungen zu treffen, um seine Pipeline zu erweitern, führen diese Parameter zu kontinuierlichen Anpassungen unserer Pläne.
Für diejenigen, die uns regelmäßig folgen, teile ich, dass im Rahmen der Beratungen im Verwaltungsrat von CLINUVEL makroökonomische Fragen wie das Handelsungleichgewicht zwischen China und den USA und Europa sowie die anhaltenden Spannungen im asiatisch-pazifischen Raum und im Südchinesischen Meer unsere Aufmerksamkeit auf sich ziehen.
Gegenwärtig zielt die Diskussion in demokratischen Ecken der Verwaltung darauf ab, Wege zu finden, die Listenpreise zu begrenzen und gleichzeitig dem Patienten zu helfen.
US-VERTRIEB
Dr Linda Teng, Direktorin für nordamerikanische Operationen
Dr Linda Teng, Direktorin für nordamerikanische Operationen
Obwohl die meisten US-Bundesstaaten nur in begrenztem Umfang tätig sind, macht unser Vertriebsteam in der heutigen Zeit bessere Fortschritte als erwartet.
Wir sehen einen stetigen Anstieg der US-Versicherer, die an der SCENESSE®-Behandlung (Afamelanotid 16 mg) teilnehmen. Täglich verwalten unsere Teams die administrativen Anforderungen aus den Anträgen auf „vorherige Genehmigung“ jedes einzelnen EPP-Patienten und unterstützen Fachzentren, wenn sie auf Verzögerungen und Schwierigkeiten mit Versicherern stoßen. Unter strikter Einhaltung der Datenschutzbestimmungen und des Gesetzes über die Portabilität und Rechenschaftspflicht von Krankenversicherungen (HIPAA) von 1996 können unsere Teammitglieder direkt helfen, ohne die persönlichen und medizinischen Daten zu gefährden. Dieser Spagat erfordert Dokumentation, Datenbanken und häufige Prüfung.
Der eindeutige J-Code wurde SCENESSE® am 1. Januar 2021 zugewiesen, und seitdem sind einige Änderungen aufgetreten.
Erstens wird in einigen Fällen jetzt eine vorherige Genehmigung pro Jahr erteilt, wodurch der bürokratische Aufwand für die Beantragung einer vorherigen Genehmigung vor jedem Implantat entfaellt. Einige Versicherungsgruppen begannen, PA für die Dauer von fünf Jahren festzulegen.
Zweitens stellen wir fest, dass die Zentren ihren Verwaltungsaufwand entlastet haben, um mehr Zeit mit Patienten zu verbringen.
Schließlich werden die Verschreibungszentren bei der Abwicklung der Verwaltungsaufgaben der Patienten besser und schneller, nachdem sie die erste Lernphase der Verwaltung und Handhabung von SCENESSE® durchlaufen haben.
In der nächsten Phase müssen unsere Teams einen behandlungsspezifischen CPT®-Code (Current Procedural Terminology) sichern. Obwohl dies normalerweise mehr als zwei Jahre dauert, haben wir es geschafft, dies um ein Jahr zu beschleunigen.
Ein CPT®-Code ermöglicht eine Reihe von Codes, Beschreibungen und Richtlinien zur Beschreibung medizinischer Verfahren und Dienstleistungen für die Bearbeitung von Ansprüchen, die Durchführung von Forschungsarbeiten, die Bewertung der Inanspruchnahme des Gesundheitswesens sowie die Entwicklung medizinischer Richtlinien und anderer Formen der Dokumentation des Gesundheitswesens.
Das CPT®-Codesystem wurde als Teil des Centers for Medicare & Medicaid Services (CMS), des HCPCS (Common Procedure Coding System) für das Gesundheitswesen, übernommen. Der HCPCS-Codesatz ist in zwei Hauptteilsysteme unterteilt: (1) Stufe I des HCPCS, die das CPT® umfasste, und (2) Stufe II des HCPCS. CPT®-Codes der Stufe I sind fünfstellige numerische Codes, mit denen medizinische Verfahren oder Dienstleistungen beschrieben werden, die von Angehörigen der Gesundheitsberufe durchgeführt werden.
Letztendlich ist die American Medical Association (AMA) für das Hinzufügen, Löschen, Überarbeiten und jährliche Aktualisieren des CPT®-Codesystems verantwortlich. Im Rahmen der HIPAA hat das Ministerium für Gesundheit und menschliche Dienste CPT® und HCPCS als nationale Standards für die elektronische Übertragung von Gesundheitsinformationen festgelegt.
Jedem medizinischen, diagnostischen oder chirurgischen Eingriff oder jeder medizinischen Dienstleistung ist ein CPT®-Code zugewiesen. Diese werden von Angehörigen der Gesundheitsberufe, Krankenhäusern, Kliniken und Versicherungsunternehmen verwendet, um Gesundheitsdienstleistungen und -verfahren in Bundesprogrammen und durch gewerbliche und / oder private Versicherer zu identifizieren. CPT®-Codes werden auch von Versicherern verwendet, um den Betrag zu bestimmen, den ein medizinisches Fachpersonal als Erstattung erhält, angesichts des Krankenversicherungsschutzes und der Vereinbarung, die das Zentrum mit dem Gesundheitsdienstleister getroffen hat.
Das US-Team ist dabei, bei der AMA einen neuen CPT®-Code für das Verfahren der SCENESSE®-Verwaltung anzufordern. Durch den Erhalt eines eindeutigen CPT®-Codes für die SCENESSE®-Verwaltung wird die vorherige Genehmigung, medizinische Abrechnung und Erstattung für die EPP-Fachzentren erleichtert und beschleunigt. Vor allem wird die Kombination von J-Code und CPT®-Code SCENESSE® als Standard für die Versorgung von US-Versicherern eingefuehrt, die es in ihre Liste der erstattungsfähigen Arzneimitteltherapien aufnehmen.
Mit zunehmendem Wissen und Erfahrung über SCENESSE® steigt auch die Anzahl der registrierten Patienten, während der einfache Zugang zur Behandlung adressiert wird. Mit der Bereitstellung der Behandlung innerhalb eines Radius von dreieinhalb Stunden für die Mehrheit der Patienten nähern wir uns unserem Ziel, landesweit ausreichende Optionen bereitzustellen.
Parallel dazu sind wir dabei, in den USA eine Struktur aufzubauen, die es CLINUVEL ermöglicht, künftig mehr Arzneimittel zu handhaben und zu vertreiben. Hierzu folgen wir einem umfassenden Plan, um alle erforderlichen pharmazeutischen Lizenzen in jedem der Schlüsselstaaten zu erhalten.
Eine erste sorgfältige Bewertung zeigt, dass die Zahlungen in den USA monatlich schwanken und von jedem Versicherer stark abhängen. Die größeren Versicherer scheinen sich an Zahlungsbedingungen von mehr als 120 Tagen zu halten, während sich kleinere an 90 Tage halten. Die erhaltenen Zahlungen variieren ebenfalls je nach Staat, es wurden jedoch bisher keine Forderungsausfälle verbucht.
Der eindeutige
J-Code wurde SCENESSE® am 1. Januar 2021 zugewiesen, und seitdem sind einige Änderungen aufgetreten.
Vitiligo Programm
Dr Linda Teng, Direktorin für nordamerikanische Operationen
Seit 2016 hat die US-amerikanische Gesundheitsbehörde FDA (Food and Drug Administration) öffentliche Treffen im Stil eines Rathauses eingeführt, um ausgewählte unbehandelte Krankheiten zu erörtern, wobei der Schwerpunkt auf patientenbezogenen Fragen zu neuen Arzneimitteltherapien liegt. Wie wir bereits berichtet hatten, war das EPP-Workshop-Treffen im Oktober 2016 die erste dieser Regulierungsinitiativen. An diesem Tag versammelten sich 150 EPP-Familien, um ihre Erfahrungen mit der Krankheit sowie die Auswirkungen seit ihrer Kindheit auszudrücken. Viele Interessengruppen waren weit gereist, um an dem Treffen in Maryland teilzunehmen.
Am 8. März veranstaltete das FDA-Zentrum für Arzneimittelbewertung und -forschung ein erstes Webinar, in dem Patienten eingeladen wurden, die Auswirkungen von Vitiligo (Pigmentverlust) auf ihr Leben, ihre Erfahrungen mit verfügbaren Behandlungen und die Erwartungen für Kuenftige zu diskutieren. Alle Stakeholder (mit Ausnahme der Pharmaindustrie), die als patientenorientierte Arzneimittelentwicklung in Vitiligo eingeführt wurden, wurden gebeten, an diesem Tag teilzunehmen.
In einem vierstündigen Treffen hatten eine große Anzahl von Patienten, Eltern und Interessengruppen die Möglichkeit, ihre Version der Auswirkungen des Pigmentverlusts auf ihr Leben zu teilen, einschließlich ihrer verringerten Chance, eine Beschäftigung zu finden und ein sozial verträgliches Leben zu führen.
Die 700 Teilnehmer und Gutachter der FDA hatten Patienten gesehen und aus erster Hand von der stigmatisierenden Natur der Krankheit gehört. Die Zuschauer an diesem Tag waren erstaunt gewesen, wenn sie erfahren hätten, wie sich jeder Einzelne mit dem Fortschreiten der Depigmentierung abgefunden hat. Was normalerweise als anfängliche kleine vitiliginöse Läsion entdeckt wurde, war häufig zu einer schnellen Ausbreitung großer Teile der Haut geworden. Viele farbige Patienten gaben an, mehr als 80% der Pigmentierung des Körpers verloren zu haben, buchstäblich „weiß“ geworden zu sein und dadurch ihre Identität verloren zu haben. Starke Emotionen und Verzweiflung wurden durch das Live-Streaming gesehen.
Die psychosozialen Auswirkungen, der Verlust des Selbstwertgefühls und die Selbstmordgedanken wurden ausdrücklich erwähnt, als die vielen Zeugnisse von Patienten und Eltern eingingen.
Die Mehrheit der eingeladenen Personen auf dem Bildschirm waren farbige Patienten. Während bei dunkel Pigmentierten der Pigmentverlust am offensichtlichsten ist, waren rassistische Uebergriffe bei Patienten ein zusätzlicher Faktor bei den meisten „Vitiligo-Lebenswegen“.
Die Eltern sprachen darüber, dass ihre Kinder wegen des entstellenden Verlusts der Gesichtspigmentierung gemobbt wurden, und andere Patienten äußerten, dass sie nach einem persönlichen Gespräch nicht die gewünschte berufliche Position erreicht hätten, da später festgestellt wurde, dass der Arbeitgeber befürchtete, dass die Einstellung eines Vitiligo Mitarbeiters die Kundschaft abschrecken und schlecht für das Geschäft sein koennte.
Monatelang hatten unsere wissenschaftlichen und klinischen Teams dieses Treffen erwartet, da sie gespannt waren, ob neue Fakten zu unserer nächsten FDA-Diskussion – später in diesem Jahr – über das endgültige Protokolldesign für eine Phase-IIb / III-Studie beitragen würden.
An diesem Tag stellte die FDA in verschiedenen von Patienten geführten Diskussionsrunden vorgegebene Fragen und bot damit eine Plattform, um Klarheit zu bestimmten Themen zu schaffen. Wir teilen eine Reihe ergreifender Antworten auf die Fragen der FDA, die aus diesen Stakeholder-Sitzungen hervorgegangen sind:
1. Der US-amerikanische Vitiligo-Sprecher und Nachrichtensprecher Lee Thomas sprach im Namen der Patienten darüber, dass das Treffen von der FDA als erste Anerkennung dafür angesehen wurde, dass Vitiligo keine kosmetische, sondern eine stigmatisierende Krankheit ist, die von der Gesellschaft und den Aufsichtsbehörden ernst genommen werden muss und die zuvor keine nationale Aufmerksamkeit bekommen hatten.
2. Die meisten farbigen Patienten sind selbstbewusst und erfahren Missbrauch, Diskriminierung und Vermeidung durch ihre Umgebung.
3. Die FDA und die Pharmaunternehmen sollten nicht nur auf die Entwicklung von Therapien achten, sondern auch auf die psychosozialen Auswirkungen von Vitiligo.
4. Ein häufiges Problem und Problem für Vitiligo-Patienten ist die Tendenz, Sonnenbrand zu erleiden, während mineralische Sonnenschutzmittel keinen Schutz bieten.
5. Ein häufiges und nicht gemeldetes Problem für Patienten ist der häufige Juckreiz der Vitiligo-Läsionen.
6. Der Pigmentverlust im Gesicht ist am einflussreichsten, da das Gesicht das Merkmal ist, das für die tägliche Kommunikation von zentraler Bedeutung ist.
7. Medikamente, die das Immunsystem möglicherweise systemisch oder lokal unterdrücken, werden als Risiko angesehen, da man die möglichen Langzeiteffekte nicht kennt.
8. Heilung wäre ein Ziel, aber jede Therapie, die die Belastung durch schmalbandiges UVB (NB-UVB) verringert, wäre sehr hilfreich. Da Patienten nach NB-UVB 12 bis 18 Monate lang dreimal pro Woche die Dermatologieklinik aufsuchen müssen, können sie häufig nicht teilnehmen, was wiederum zu einem Mangel an Behandlungseffekt führt.
9. Ein Mindestziel für eine neue Therapie wäre die Repigmentierung von mehr als 50% der Vitiligo-Läsionen im Gesicht.
10. Ein verzweifelter Ruf an die FDA und die Pharmaunternehmen, eine wirksame Therapie für Erwachsene und Kinder zu entwickeln.
Die offene Prozessliste der FDA endet am 10. Mai. Bis dahin haben alle Patienten und die Öffentlichkeit die Möglichkeit, neue relevante Fakten über Vitiligo auszutauschen.
Das Team von CLINUVEL wird sich noch einmal mit der FDA treffen, um das endgültige Protokolldesign für Vitiligo zu vereinbaren, bei dem alle während des Workshops vom 8. März zusammengefassten Aspekte berücksichtigt werden.
Mein Eindruck des Tages war, dass die FDA Vitiligo jetzt mit Sicherheit ernst nimmt, und obwohl noch nie eine zugelassene Therapie für die Krankheit zur Verfügung gestellt wurde, bin ich der festen Überzeugung, dass die Agentur ihr Engagement zur Unterstützung der Arzneimittelentwicklung für diese Patienten offen zum Ausdruck gebracht hat.
Ich habe auch von dem Treffen mitgenommen, dass immunsuppressive Therapien in der Entwicklung für Vitiligo ein echtes Problem für Patienten sind, und die medizinische Gemeinschaft wird diese sorgfältig prüfen, bevor sie einem Patienten verabreicht werden. Wenn und wann Immunmodulatoren die behördliche Zulassung für Vitiligo erhalten, wird die Vorsicht und die Besorgnis über die langfristigen Auswirkungen weit verbreitet sein.
Wichtig ist, dass der Workshop erneut das lebenslange Risiko eines Sonnenbrands bei Vitiligo-Patienten und die Notwendigkeit eines Lichtschutzes hervorhob.
Überraschenderweise sind die Symptome eines anhaltenden Juckreizes bei Vitiligo bisher nicht gut beschrieben und bei der Arzneimittelentwicklung nicht besonders ausgeprägt.
Obwohl die FDA NB-UVB nicht als Standardtherapie bei generalisiertem Vitiligo (der häufigsten klinischen Darstellung der Krankheit) zugelassen hat, ist es derzeit die bevorzugte Behandlung für Patienten mit Farbe. Einige Patienten haben sich für den Heimgebrauch auf tragbare UV-emittierende Geräte verlassen, um zeitaufwändige Besuche in Arztpraxen zu vermeiden. Es wird jedoch berichtet, dass häufige Verbrennungsunfälle aufgetreten sind.
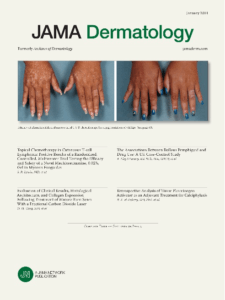
Wir beziehen uns auf unsere Vitiligo Scientific Communiqués, um unsere Arbeit und den wissenschaftlichen Fortschritt bei generalisiertem Vitiligo zu überprüfen. Die Verwendung von Afamelanotid in Kombination mit NB-UVB wurde zuerst in JAMA Dermatology und später im Journal der American Academy of Dermatology veröffentlicht. Am 29. Oktober 2020 haben wir in unserem Strategic Update I eine Zusammenfassung von Vitiligo bereitgestellt.
Die Gesamtbehandlung von Vitiligo-Patienten erfordert eine psychosoziale Bewertung und mögliche Beratung, um psychischen Stress während der Behandlung zu lindern, was als möglicher Co-Faktor bei der Entwicklung von Vitiligo beschrieben wird.
Unsere Teams zeigten sich begeistert von der Initiative der FDA, endlich den Input der Patienten einzuholen, um mehr über Vitiligo zu erfahren und die Arzneimittelentwicklung zu unterstützen. Wir werden wieder berichten, sobald das letzte Treffen des Typs C mit der FDA stattgefunden hat und eine Einigung über ein Protokoll erzielt wurde.
Aktuelle Vitiligo-Behandlungen (USA)
Off-label (nicht für
Vitiligo zugelassen):
– Kortikosteroide
– (aktuell)
– Calcineurin-Inhibitoren
– (aktuell)
– Vitamin D-Derivate
– PUVA-Psoralen
– Schmalband-UVB
– Synthetisches Prostaglandin-F2-
alpha-Analogon
– Janus Kinase 1 und 2 Inhibitor
-Depigmentierungsmittel
– Prostaglandine
(topisches Gel)

“Ich habe in einer Gesellschaft, die sich auf die physische Erscheinung konzentriert,
mit vielen Herausforderungen zu kämpfen gehabt. Dazu gehören unangenehme Blicke, Fingerzeig und Menschen, die sich weigern, meine Haut zu berühren, aus Angst, dass sie ansteckend und verletzend ist.”
– Dhyana lebt seit 11 Jahren mit Vitiligo.
EU-VERTRIEB
Lachlan Hay, Direktor für Globale Operationen
Die in ganz Europa eingeführten Ausgangssperren und Beschränkungen wirkten sich weiterhin auf das tägliche Leben der EPP-Patientengemeinschaft sowie der Ärzte aus, mit denen wir zusammenarbeiten. Unsere Mitarbeiter arbeiten abhaengig von deren Verfügbarkeit und ein Großteil der Überwachung nach der Autorisierung erfolgt derzeit aus der Ferne. Trotz der Herausforderungen ist es ermutigend berichten zu koennen, dass die meisten aktiven europäischen EPP-Expertenzentren mit der Behandlung von Patienten für das Kalenderjahr begonnen haben und neue Zentren in Betrieb genommen werden sollen.
In ganz Europa hat das Team weiterhin die von der EMA im Jahr 2014 auferlegten Anforderungen nach dem Inverkehrbringen befolgt, um die Verschreibung von SCENESSE® für EPP-Patienten zu überwachen. Hier liegt der Schwerpunkt auf dem langfristigen Sicherheitsprofil des Produkts sowie auf dem Management spezifischer identifizierter und potenzieller Risiken im Rahmen eines vereinbarten Risikomanagementplans. Es ist ein Beweis für die langjährigen Beziehungen zu akademischen und klinischen Experten, die ihre Patienten versorgen, sowie für das Engagement des CUV-Teams, dass sich die Mehrheit der EPP-Patienten für die Teilnahme an der Sicherheitsstudie nach der Zulassung (PASS) entscheidet. Sie stimmen zu, dass ihre Daten unter einem Pseudonym in das Europäische EPP-Krankheitsregister hochgeladen werden. Auf diese Weise erhält unser Team nahezu in Echtzeit Feedback zum Medikamentenkonsum sowie die Möglichkeit, der EMA jährlich datenreiche Berichte zur Verfügung zu stellen.
Der PASS-Jahresbericht ist eine wichtige Aufgabe unseres Teams für klinische Operationen. Wie jeder statistische Bericht beruht er nicht nur auf der Qualität und Genauigkeit der Daten und der Analyse, sondern auch auf einem grundlegenden Verständnis dessen, was diese Ergebnisse zeigen. Anders ausgedrückt, ohne Expertenwissen darüber, wie EPP-Patienten in der Klinik behandelt werden, sind die Statistiken von begrenztem Nutzen. Sich Jahr für Jahr auf ein konsistentes Team und internes Wissen verlassen zu können, bietet einen hohen Wert.
Der jüngste Bericht – der fünfte, der im Dezember fertiggestellt wurde und Daten bis zum 22. Juni 2020 enthält – gibt einen Einblick in die fortlaufende Verwendung von SCENESSE® in ganz Europa. Ausschlaggebend für unsere Analysen ist, dass sich das Sicherheitsprofil des Produkts sowohl im Vergleich zu den Vorjahren als auch im Rahmen des zugelassenen Produktetiketts als konsistent erwiesen hat. Drei von fünf Patienten berichten von Nebenwirkungen der Behandlung (Übelkeit und Kopfschmerzen sind am häufigsten), aber die meisten dieser Reaktionen sind mild und vorübergehend (innerhalb von 24 bis 48 Stunden nach der Behandlung).
Die Anzahl der Patienten, die weiterhin SCENESSE® erhalten, ist im Jahresvergleich hoch: Unsere neuesten Analysen zeigen, dass die jährliche Behandlung zu 94% eingehalten wird. Messungen der Lebensqualität von Patienten im Vergleich zum Ausgangswert zeigen eine Verbesserung des Ansprechens auf SCENESSE® sowie eine Verbesserung gegenüber dem Vorjahr in den Frühlings- und Sommermonaten, wenn bei Patienten das höchste Risiko für phototoxische Reaktionen besteht.
Der bei der EMA eingereichte fünfte Jahresbericht spiegelt die klinischen Beweise und von Experten begutachteten Zeitschriftenartikel wider, die von europäischen EPP-Expertenzentren erstellt wurden und die eine allgemeine Verbesserung des Lebens der Patienten und die Fähigkeit zur Führung einer „normalen“ Existenz erklären, die bisher für unmöglich gehalten wurde. Dies bietet zwar den Komfort, dass wir den Patienten einen erheblichen und echten Nutzen bieten, aber unsere Teams setzen sich weiterhin dafür ein, dass wir EPP-Patienten lebenslang versorgen können.
Die Herausforderungen der Pandemie und der sich entwickelnden regulatorischen Landschaft haben sich auf das gesamte Unternehmen ausgeweitet. Änderungen sind erforderlich, um die Einhaltung in einem sich entwickelnden und unvorhersehbaren Umfeld zu erleichtern. Die Voraussicht unseres Teams, die Zusammenarbeit mit den Aufsichtsbehörden und die Zusammenarbeit mit unseren Vertriebspartnern haben die Verfügbarkeit der Behandlung erleichtert.
Ein Beispiel ist der Ansatz zur Chargenfreigabe von fertigen pharmazeutischen Produkten. Die Prozesse der Chargenfreigabe wurden kürzlich im Zusammenhang mit COVID-19-Impfstoffen in einigen Medien erwähnt, aber nur wenige haben die Rolle der Chargenfreisetzung bei der Lieferung der spezialisierten Arzneimittel beachtet. Im Kern erfordert die Chargenfreigabe eine unabhängige „qualifizierte Person“ (QP), die die Dokumentation analysiert und zertifiziert und bestätigt, dass ein Arzneimittel die Qualität und die Spezifikationen erfüllt, die erforderlich sind, um diese Charge für die Verwendung durch den Patienten verfügbar zu machen. Sicherheit ist das zentrale Anliegen – ohne ein konsistentes Qualitätsprodukt kann ein Unternehmen das Sicherheitsprofil eines pharmazeutischen Produkts nicht gewährleisten. Wie zu erwarten ist, ist diese Aufgabe stark reguliert und wird nach strengen Qualitätsmanagementprotokollen durchgeführt, die den physischen Ort bestimmen, an dem die Freigabe erfolgt – eine zertifizierte GMP-Site (Good Manufacturing Practices). Dieser Ansatz stellt sicher, dass der Freigabeprozess konsistent und kontrolliert ist. Im vergangenen Jahr war die Möglichkeit, GMP-Standorte zu besuchen und zu prüfen, in vielen Ländern jedoch eingeschränkt (wenn nicht sogar völlig unmöglich), was eine Überarbeitung der Art und Weise und des Ortes der Chargenfreigabe sowie der allgemeinen Anforderungen an Qualitätssysteme erforderlich machte. Die Erweiterung eines Qualitätssicherungssystems zur Erleichterung der Fernfreigabe von Chargen mag zwar einfach erscheinen, ist jedoch eine entscheidende Änderung des regulatorischen Denkens, die es CLINUVEL jedoch ermöglicht hat, die Arzneimittelversorgung fortzusetzen. Man sieht voraus, dass diese praktische Veränderung – und andere, die durch die Pandemie hervorgerufen wurden – noch lange nach Aufhebung der Beschränkungen fortgesetzt wird. Neue Umgebungen zwingen uns, unsere Systeme zu überdenken und neu zu gestalten.
Bei der Preisgestaltung von SCENESSE® in der Europäischen Union haben wir uns zum Ziel gesetzt, mit gutem Beispiel voranzugehen und die nationalen Vereinbarungen zu respektieren, die wir in den letzten Jahren getroffen haben. Diese beziehen sich auf:
I. einheitliche Nettopreise
II. Anzahl der verschreibenden EPP-Expertenzentren
III. projiziertes Volumen, Anzahl der Injektionen
IV. Anzahl der Patienten
V. Off-Label-Verwendung
VI. ausgebildete und akkreditierte Zentren und
VII. Überwachung nach dem Inverkehrbringen.
In einer Welt, in der die weit verbreitete Skepsis während der Interaktionen zwischen Versicherungsgruppen und Pharmaunternehmen dominiert, haben wir einen einzigartigen Plan entworfen, um den Zahlern einen transparenten und einheitlichen Ansatz zu demonstrieren.
In vielen dieser Diskussionen, Verhandlungen und – in einigen Fällen – Gerichtsverfahren und Berufungsgremien haben wir die Arbeitsweise von CLINUVEL dargestellt und festgelegt, wie wir einen einheitlichen Nettopreis für alle Mitgliedstaaten und die Eurozone aufrechterhalten können. Unsere Teams sind nie von diesem Prinzip abgewichen, und wir haben in den letzten vier Jahren darauf verzichtet, den Preis zu erhöhen.
Normalerweise führt die überwiegende Mehrheit der Medikamente Preiserhöhungen und Anpassungen für den indexbasierten Konsum durch. CLINUVEL korrigierte den VPI jedoch trotz der steigenden Kosten für Rohstoffe, Herstellung, Kennzeichnung, Verpackung, Vertrieb und Transport nicht. Dieser unerschütterliche Glaube an ein starkes Prinzip sorgt vielleicht fuer Kritik von Fonds und institutionellen Aktionären. Wir sind jedoch weiterhin der Ansicht, dass Transparenz in diesem Bereich einen langen Weg geht und ganz am Ende den Respekt derselben Zahler gebietet, die Verträge mit dem Arzneimittel einhalten, Firmen wie CLINUVEL.
Heute, im fünften Jahr des kommerziellen Vertriebs von SCENESSE®, können wir mit denselben Versicherern pro Land sprechen und vierteljährliche Berichte vorlegen, in denen dargelegt wird, wie wir die von 2014 bis 2021 getroffenen Vereinbarungen eingehalten haben. CLINUVEL hat weder die Anzahl der Zentren noch die Anzahl der Injektionen und Patienten ueberschritten, die in jeweils einem der europäischen Länder behandelt wurden; was mit den nationalen Angaben, die wir ab 2014 gemacht haben, uebereinstimmt.
Die allgemeine Sorge bestand, dass CLINUVEL das Medikament auf den Markt „auspeitschen“ und Off-Label-Produkte vertreiben würde. Auch hier haben wir unsere festgelegten Grundsätze und Vereinbarungen eingehalten, und es wurde kein einziges SCENESSE®-Implantat für die Off-Label-Verwendung geliefert. Ich muss diese Aussage jedoch einschränken. Unsere Teams stellten ein Off-Label-Implantat für einen Patienten mit angeborener erythropoetischer Porphyrie (CEP) zur Verfügung, der todkrank war. Wir haben dies aus Mitgefuehl getan, um versuchen, in den letzten Lebensmonaten des Patienten Lebensqualität zu schaffen.
Oft stellt sich die Frage, ob CLINUVEL daher das kommerzielle Potenzial des Afamelanotid-Arzneimittels maximiert hat. Paradoxerweise können wir von ganzem Herzen antworten, dass wir durch diese Vorgehensweise tatsächlich die Chance maximieren. Durch die Einschränkung der Verbreitung und die Verneinung der Off-Label-Nutzung haben wir das Vertrauen vieler Zahler und Versicherungsgruppen gewonnen. Dies bietet eine fruchtbare Diskussion für die kommenden Jahre und dient möglicherweise sogar als Benchmark für andere Unternehmen.
Ab September 2021 wird CLINUVEL den SCENESSE®-Preis anpassen, um die jährlichen Preiserhöhungen von mehr als 20% widerzuspiegeln, die wir in den letzten vier Jahren für die Erhöhung aller Rohstoffe und Herstellungsprozesse getragen haben. Unsere Preiserhöhung wird mit Zahlern und Versicherern besprochen und beträgt ca. 13,1%. Drei Monate vor Inkrafttreten der Preiserhöhung werden wir dies den jeweiligen Versicherungsgruppen mitteilen.
Es ist ein Beweis für die langjährigen Beziehungen zu akademischen und klinischen Experten, die ihre Patienten versorgen, sowie für das Engagement des CUV-Teams, dass sich die Mehrheit der EPP-Patienten für die Teilnahme an der Sicherheitsstudie nach der Zulassung (PASS)
Die Prozesse der Chargenfreigabe wurden kürzlich im Zusammenhang mit COVID-19-Impfstoffen in einigen Medien erwähnt, aber nur wenige haben die Rolle der Chargenfreisetzung bei der Lieferung der spezialisierten Arzneimittel beachtet.
In vielen dieser Diskussionen, Verhandlungen und – in einigen Fällen – Gerichtsverfahren und Berufungsgremien haben wir die Arbeitsweise von CLINUVEL dargestellt und festgelegt, wie wir einen einheitlichen Nettopreis für alle Mitgliedstaaten und die Eurozone aufrechterhalten können.
Expansion CLINUVEL Group
Im Jahr 2020 haben wir die zweite Afamelanotidformulierung, PRÉNUMBRA®, als Teil des Lebenszyklusmanagements des Moleküls vorgestellt. Wir haben lange geplant, das Molekül und andere Melanocortine bei lebensbedrohlichen und schweren Erkrankungen einzusetzen.
Der kommerzielle Erfolg von PRÉNUMBRA® hängt von einer Reihe von Aspekten ab. Erstens muss das Sicherheitsprofil der bei verschiedenen Erkrankungen verwendeten Produkte den bekannten Sicherheitsdaten von SCENESSE® ähneln, wie wir sie derzeit von erwachsenen Patienten mit EPP oder Photodermatosen haben.
Zweitens und von gleicher Bedeutung für die kommerzielle Verwendung des Produkts liegt unser Schwerpunkt auf der Entwicklung und Validierung von Analysemethoden. Einfacher ausgedrückt erfordert die Art und Weise, wie wir die chemischen und pharmakologischen Eigenschaften und das biologische Verhalten dieser beiden Produkte im menschlichen Blutkreislauf messen, sensible und spezifische Methoden (Assays), die von unseren Analyseteams in den Laboratorien in Singapur entwickelt wurden. Diese Aspekte und Geschäftsmöglichkeiten von PRÉNUMBRA® werden in Strategic Update II berücksichtigt.
Trotz der Möglichkeiten, die die Globalisierung durch Konnektivität bietet, sehe ich paradoxerweise starke geopolitische Trends hin zu einem Rückzug in die nationale Autarkie und in den lokalen Fokus. Ich habe nach und nach die Souveränität von Bedeutung für expandierende Organisationen wie CLINUVEL gesehen. Angesichts des Rückgangs der Volkswirtschaften, der Überschussländer, die unter sinkenden Exporten leiden, und der Auswirkungen der Abhängigkeit sollten Entscheidungen über die Zukunft von CLINUVEL und seine Risiken getroffen werden.
Der Verwaltungsrat, Berater, Rechtsteams und Manager hatten viele Jahre lang über die Möglichkeit der Fertigung diskutiert. Dafür benötigten wir Nachhaltigkeit des Geschäfts, Vertrauen in zukünftige Märkte und Analyse der aktuellen Behandlungsoptionen. Als wir unser Portfolio um OTC-Produkte – nicht verschreibungspflichtige Produkte für eine breitere Öffentlichkeit – erweitert haben, haben wir unsere Notwendigkeit bekräftigt, unabhängig zu werden und die vierte Division intern zu betreiben.
Natürlich kann darüber diskutiert werden, ob der Betrieb von Produktionsanlagen unter den gegenwärtigen wirtschaftlichen Bedingungen umsichtig ist. Bei CLINUVEL überwiegen die Vorteile jedoch deutlich die Nachteile. Es erfordert Fokus, Kostenmanagement und operatives Know-how. Durch die Fokussierung auf Produkte mit verzögerter Freisetzung, aber auch auf transdermale Formulierungen wird die Gruppe in der Lage sein, als Contract Development & Manufacturing Organization (CDMO) für andere Forschungsgruppen und Unternehmen zu produzieren. Unser Vorsitzender hat zuletzt über die Hinzufügung dieser vierten Abteilung geschrieben.
Im Fall von CLINUVEL besteht eine Synergie zwischen unserem Team bei VALLAURIX (Singapore Laboratories) und der Fertigung, während wir davon ausgehen, dass sich das Personal austauschen wird. Die Produktionsstätten werden vor Ort analytische Laboratorien umfassen, in denen Methodentransfers innerhalb der Gruppe stattfinden.
Es ist ein spannender Teil unserer Expansion, der viel Nachdenken, Aufmerksamkeit, Planung und neue Fähigkeiten erfordert hat. Die Hinzufügung neu eingestellter Manager ermöglichte Diskussionen über Design, Engineering, Ausrüstung, Prozesse und Produkte.
Im Strategic Update I vom Oktober 2020 kündigte das Unternehmen die Schaffung einer neuen Abteilung für Kommunikation, Branding und Marketing (CBM) an, die größtenteils in Großbritannien eingerichtet wird. Dieser Ansatz steht im Einklang mit der Vorgehensweise von CLINUVEL, Talente langfristig unter einem Dach aufzubauen und zu halten, anstatt sich auf externes Fachwissen zu verlassen. Ziel ist es, ein Team im Agenturstil zu schaffen, das CLINUVEL betreut und es dem Unternehmen ermöglicht, auf moderne und kreative Weise mit neuen Zielgruppen in Kontakt zu treten. Dies machte es erforderlich, der Gruppe neue Kompetenzen hinzuzufügen und in Talente und Fachkenntnisse, Software, Systeme und Ausrüstung zu investieren. Derzeit berichten wir, dass die Rekrutierung des CBM-Teams zu 80% abgeschlossen ist und vier weitere Stellen zu besetzen sind, um alle Medien- und Kommunikationsfunktionen digital ausführen zu können.
Der CBM-Abteilung wurden klare Ziele gesetzt, um die Online-Präsenz neuer Marken zu erhöhen und das Publikum mit den Projekten und Produkten anzusprechen, die wir starten möchten. Infolgedessen werden die Anleger sehen, wie sich CLINUVEL in den kommenden Monaten allmählich präsentieren wird.
Der Verwaltungsrat, Berater, Rechtsteams und Manager hatten viele Jahre lang über die Möglichkeit der Fertigung diskutiert.
Im Strategic Update I vom Oktober 2020 kündigte das Unternehmen die Schaffung einer neuen Abteilung für Kommunikation, Branding und Marketing (CBM) an, die größtenteils in Großbritannien eingerichtet wird.
INVESTOREN BEZIEHUNGEN
Malcolm Bull, Leiter Investoren Beziehungen
CLINUVEL hat im ersten Quartal 2021 weiterhin positive Nachrichten über seine Fortschritte geliefert.
Während dieses Zeitraums veröffentlichte das Unternehmen zwei wichtige finanzielle Aktualisierungen. Der erste im Januar war der Cashflow-Bericht für das Dezember-Quartal 2020 und der zweite im Februar war der Halbjahresbericht für den am 31. Dezember 2020 endenden Zeitraum. Im Vergleich zu den negativen Nettoeinnahmen aus dem gleichen Zeitraum in den Jahren 2019 und 2018. Für das Kalenderjahr 2020 erreichten die Einzahlungen ein Rekordniveau von 33,053 Mio. AUD. Für das am 31. Dezember 2020 endende Halbjahr meldete CLINUVEL den zehnten Halbjahresgewinn in Folge und einen Rekordgewinn für ein Halbjahr im Dezember.
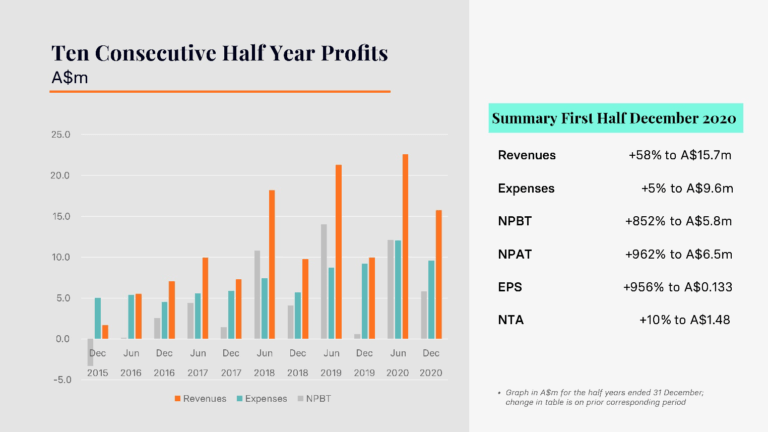
Der Umsatz stieg um 58% und die Ausgaben konnten gut um 5% gesteigert werden. Im ersten Halbjahr des Geschäftsjahres 2021 wurde ein Nettogewinn vor Steuern von 5,811 Mio. AUD erzielt.
Die Cash- und Profitergebnisse spiegeln die Normalisierung der Behandlungstätigkeit in Europa nach anfänglichen Einschränkungen der Behandlungen im Zusammenhang mit der COVID-19-Pandemie im Zeitraum März – Mai 2020 und den ersten Beiträgen aus dem Vertrieb von SCENESSE® in den USA wider.
Betriebsaktualisierung – Webinar
Das Unternehmen hat seine Kommunikation in diesem Jahr diversifiziert, indem es eine Webinar-Reihe mit operativen Updates gestartet hat, um eine alternative Form der Kommunikation über den Geschäftsfortschritt bereitzustellen, die formelle Unternehmensankündigungen ergänzt. Im ersten Webinar im Februar berichteten die Führungskräfte von CLINUVEL über die Halbjahresergebnisse bis zum 31. Dezember 2020 und informierten über die Verbreitung von SCENESSE® und die Erweiterung des Forschungs- und Entwicklungsprogramms. Das Webinar wurde gut aufgenommen, mit positiven Kommentaren zum Format der Diskussion sowie der effektiven Verwendung von Grafiken als Ergänzung zum Kommentar. Wir finden dieses Feedback ermutigend, diese Initiative fortzusetzen.
Wir werden die Aktionäre vor der Aufzeichnung des nächsten Webinars erneut um Fragen bitten, um das Gespräch zu leiten.
Andere Ankündigungen
Im Februar kündigten wir die Gewährung des Marktzugangs für SCENESSE® in Israel an. Dies ist die erste Genehmigung für die nationale Erstattung der Behandlungskosten für SCENESSE® im Nahen Osten. Im vergangenen Monat haben wir die Erweiterung des DNA-Reparaturprogramms angekündigt, um SCENESSE® bei Patienten mit der Xeroderma pigmentosum-Variante XP-V zu evaluieren. Die Erweiterung des Programms basiert auf laufenden Diskussionen mit klinischen und akademischen Experten, die die Verwendung des Arzneimittels sowohl in der XP-C- als auch in der XP-V-Komplementationsgruppe unterstützen. Es gibt eine starke wissenschaftliche Begründung für die Verwendung des Arzneimittels in XP-C und XP-V, und es gibt genügend Unterstützung, um diese logische Erweiterung vorzunehmen. In der letzten Woche haben wir unsere Expansion mit einer vierten Division, der Fertigung, vorgestellt.
Alle Ankündigungen des Unternehmens sind auf der CLINUVEL-Website verfügbar.
Das zweite strategische Update soll in den kommenden Wochen veröffentlicht werden und auf dem strategischen Update vom Oktober 2020 aufbauen.
Teilnahme an Veranstaltungen
Im Jahr 2020 nahmen wir an acht Konferenzen teil und präsentierten uns auf sechs, hauptsächlich virtuell, wie es zur vorübergehenden Norm geworden ist.
Unser Ziel ist es, neue potenzielle Investoren zu erreichen, indem wir die CLINUVEL-Geschichte erzählen und die zwingenden Gründe vermitteln, uns als Investition zu betrachten und bestehende Investoren über den Fortschritt des Unternehmens zu informieren.
CLINUVEL hat in diesem Jahr bisher an drei bedeutenden internationalen Konferenzen teilgenommen. Die erste war die JP Morgan Healthcare Conference im Januar. Wir präsentierten uns dann auf der HC Wainwright Bioconnect-Konferenz im Januar und der Daiwa Investment Conference in Tokio im März. All dies waren virtuelle Konferenzen, und obwohl dies das Ausmaß des Beziehungsaufbaus einschränkt, das normalerweise durch persönliche Treffen erreicht wird, freuen wir uns, neue Investoren zu erreichen und Einzelgespräche mit denjenigen zu führen, die am meisten an CLINUVEL interessiert sind.
Die Präsentationen behandelten die Entwicklung von CLINUVEL durch jahrelange Arzneimittelentwicklung bis hin zu einer positiven Cash- und Gewinngenerierung und einer starken Finanzlage aus dem kommerziellen Betrieb. Die Rolle des hartnäckigen Charakters des Unternehmens bei diesen Errungenschaften und die Ausweitung des Forschungs- und Entwicklungsprogramms mit den geplanten Ergebnissen für 2021 wurden ebenfalls behandelt. Die Stärken und der Charakter von CLINUVEL, die auf den Konferenzen vorgestellt wurden, werden im Folgenden gezeigt, um zu veranschaulichen, wie wir das Unternehmen externen Stakeholdern präsentieren.

Die Präsentation und unsere Geschichte wurden mit einem Follow-up von institutionellen Investoren gut aufgenommen. Dies erfordert unsere Zeit und weitere Diskussionen.
Der Kalender der geplanten Veranstaltungen für 2021 ist unten zu Ihrer Information angegeben. Eine Anzahl muss noch bestätigt werden.
| Monat | geplante Veranstaltungen |
|---|---|
| Januar | JP Morgan Healthcare Konferenz, San Francisco |
| HC Wainwright Bioconnect Investment Konferenz | |
| März | Daiwa Investment Konferenz, Tokyo |
| Mai | UBS Global Healthcare Konferenz (noch zu bestätigen) |
| Europäische Gesellschaft für pädiatrische Dermatologie, 20. Jahrestagung (noch zu bestätigen) | |
| Juni | Jefferies Global Healthcare Konferenz |
| Goldman Sachs Global Healthcare Konferenz (noch zu bestätigen) | |
| Symposium der American Society for Photobiology 2021 (noch zu bestätigen) | |
| September | Goldman Sachs Europäische Medtech & Healthcare Konferenz (noch zu bestätigen) |
| HC Wainwright Global Investment Konferenz (noch zu bestätigen) | |
| Oktober | Morgans 5. Jahreswert in der Vines Investor Konferenz (noch zu bestätigen) |
| Citis 12. jährliche Investitionskonferenz in Australien und Neuseeland (noch zu bestätigen) | |
| November | Jefferies London Healthcare Konferenz (noch zu bestätigen) |
| XII. Internationaler Kongress für Dermatologie |
Das Webinar wurde gut aufgenommen, mit positiven Kommentaren zum Format der Diskussion sowie der effektiven Verwendung von Grafiken als Ergänzung zum Kommentar.
Summary
COVID besetzt weiterhin große Teile der Welt, während Australien und Neuseeland die Ausbreitung des Virus offenbar effektiv gemeistert haben.
Unsere singapurischen Labors (VALLAURIX) arbeiten wieder in Vollzeit und arbeiten eine Schicht, seit der Leistungsschalter angehoben wurde, und es gibt keine nationale Unterscheidung mehr zwischen wesentlichen und nicht wesentlichen Dienstleistungen. Unsere Mitarbeiter haben während der COVID-Beschränkungen neue Mitglieder aufgenommen, und die Integration ist dank unserer effizienten Prozesse nahtlos.
In Europa verhängen England, Frankreich, Deutschland, Italien und die Niederlande Ausgangssperren und Beschränkungen außerhalb der Bürozeiten, und es herrscht große Unsicherheit darüber, ob das Wirtschaftsleben rasch wieder aufgenommen wird. Ich glaube, dass 70% der Bevölkerung geimpft werden müssen, bevor die EU-Regierungen über die Aufhebung von Beschränkungen nachdenken.
Kürzlich wurde in einer Diskussion mit einem australischen Fondsmanager das Thema angesprochen, was der wichtigste Faktor für die bisher erfolgreiche Reise von CLINUVEL war. Ohne Zeit für die Vorbereitung des Treffens zu haben, antwortete ich ihm mit einer Lieblingsparabel, die von einem jungen, temperamentvollen Anwalt und großen Amerikaner, Abraham Lincoln, ausgesprochen wurde: „Denken Sie immer daran, dass Ihre eigene Entschlossenheit zum Erfolg wichtiger ist als alles andere.“
Der flüchtige Erfolg von Arzneimitteln zwingt mich, von unserem günstigen Status abzuweichen, aber ich tröste mich mit dem Wissen, dass unser Team Belastbarkeit und Einfallsreichtum gezeigt hat, um Hindernisse zu überwinden, bei denen die meisten anderen aufgegeben hätten. Während ich es ablehne, in öffentlichen Unternehmen eine Anleitung zu geben, ist die Betrachtung des konsequenten menschlichen Verhaltens und der Ausführung in den letzten 15 Jahren vielleicht die Prophezeiung, die der Prophezeiung am nächsten kommt. Wir sind auf eine große Anzahl von Fachleuten angewiesen, die bereit sind, ihre Zeit und Energie für große Zwecke einzusetzen.
Mit CLINUVEL sind wir auf einer Odyssee, haben in den Abgrund gestarrt und auf Gipfel geblickt. Ich bin mir sicher, dass noch eine Reihe weiterer Herausforderungen vor uns liegen, aber aufgrund der Ausführung meiner leitenden Angestellten, eines einvernehmlichen Verwaltungsrats, bin ich überzeugt, dass wir alle unsere Ziele rechtzeitig erreichen werden. Ich führe ein Leben nach dem Prinzip, dass eine konzentrierte Anstrengung Ergebnisse liefert, sobald der menschliche Geist auf bestimmte Aufgaben eingestellt ist. Dies ist die Kraft von Individuen, die diese echten Überzeugungen teilen. Das haben wir bei CLINUVEL.
Wir werden uns in den nächsten Wochen zum Strategic Update II wiedersehen, wo wir weitere Hinweise zur Expansion von CLINUVEL und zu den diesen Entscheidungen zugrunde liegenden Gründen geben.
Philippe Wolgen
Ich tröste mich mit dem Wissen, dass unser Team Belastbarkeit und Einfallsreichtum gezeigt hat, um Hindernisse zu überwinden, bei denen die meisten anderen aufgegeben hätten.
Share Price
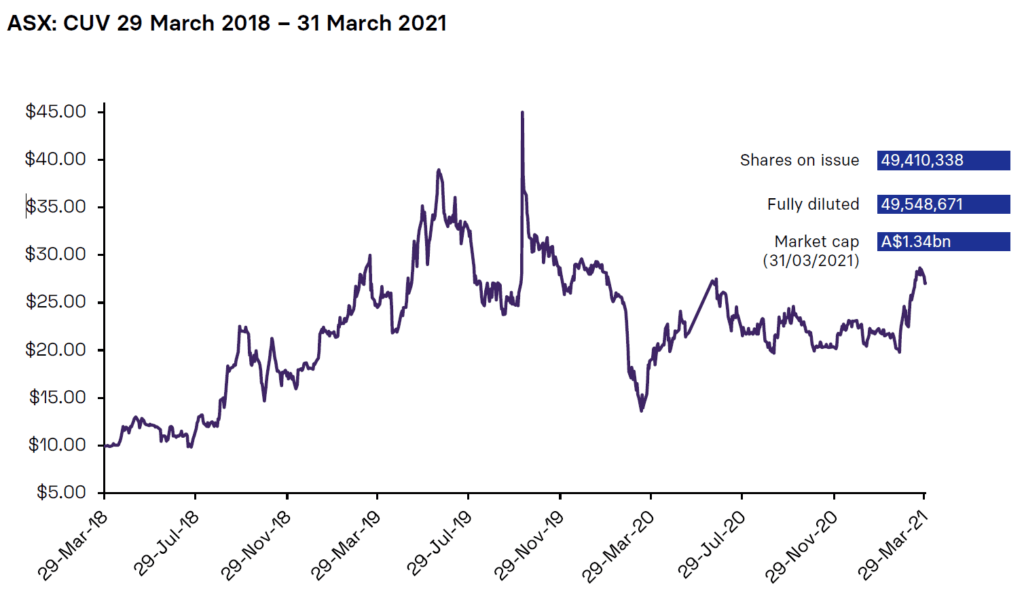
Autorisiert für ASX-Freigabe durch den Verwaltungsrat von CLINUVEL PHARMACEUTICALS LTD.
Zukunftsgerichtete Aussagen
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen, die die aktuellen Überzeugungen und Erwartungen des CLINUVEL-Managements widerspiegeln. Aussagen können eine Reihe bekannter und unbekannter Risiken beinhalten, die dazu führen können, dass unsere zukünftigen Ergebnisse, Leistungen oder Errungenschaften erheblich von denen abweichen, die in solchen zukunftsgerichteten Aussagen ausgedrückt oder impliziert werden. Wichtige Faktoren, die solche Unterschiede verursachen oder dazu beitragen könnten, sind Risiken im Zusammenhang mit: unsere Fähigkeit, pharmazeutische Produkte zu entwickeln und zu vermarkten, die COVID-19-Pandemie, die die Lieferkette für einen längeren Zeitraum beeinflusst, einschließlich unserer Fähigkeit, biopharmazeutische Produkte zu entwickeln, herzustellen, zu vermarkten und zu verkaufen; Wettbewerb um unsere Produkte, insbesondere SCENESSE® (Afamelanotid 16mg); unsere Fähigkeit, erwartete Sicherheits- und Wirksamkeitsergebnisse durch unsere innovativen F&E-Bemühungen zu erzielen; die Wirksamkeit unserer Patente und anderer Schutzmaßnahmen für innovative Produkte, insbesondere im Hinblick auf nationale und regionale Unterschiede in den Patentgesetzen; unsere potenzielle Exposition gegenüber Produkthaftungsansprüchen in dem Umfang, der nicht durch Versicherungen abgedeckt ist; verstärkte staatliche Kontrolle in Australien, den USA, Europa und Japan unser Engagement gegenüber Währungsschwankungen und -beschränkungen sowie Kreditrisiken; die Auswirkungen von Reformen der Gesundheitsregulierung und der Arzneimittelpreise und -erstattung; dass das Unternehmen unerwartete Verzögerungen bei der ausgelagerten Herstellung von SCENESSE® verursachen kann, was dazu führen kann, dass es nicht in der Lage ist, seine kommerziellen Märkte und/oder klinischen Testprogramme zu liefern; alle Verstöße gegen staatliche Zahlungsverkehrssystem (d. h. Medicare) Melde- und Zahlungsverpflichtungen; Unsicherheiten im Zusammenhang mit den gesetzlichen und regulatorischen Wegen für die Registrierung und Zulassung biotechnologischer Produkte; Entscheidungen der Aufsichtsbehörden über die Zulassung unserer Produkte sowie deren Entscheidungen in Bezug auf Etikettenansprüche; jede Nichtbeachtung oder Gewinnung von Schlüsselpersonal und Führungstalenten; die Auswirkungen eines umfassenderen Wandels in der pharmazeutischen Industrie und verwandten Industrien; mögliche Änderungen der Steuerverbindlichkeiten oder -gesetze; Umweltrisiken; und andere Faktoren, die in unserem Jahresbericht 2020 erörtert wurden. Zukunftsgerichtete Aussagen beziehen sich nur auf das Datum, an dem sie abgegeben werden, und das Unternehmen übernimmt keine Verpflichtung, außerhalb der nach den geltenden Gesetzen oder den einschlägigen Kotierungsregeln der Australischen Wertpapierbörse erforderlichen Aussagen jede zukunftsgerichtete Erklärung zu aktualisieren oder zu überarbeiten, sei es aufgrund neuer Informationen, zukünftiger Ereignisse oder auf andere Weise. Weitere Informationen zu den Prognosen und Schätzungen erhalten Sie auf Anfrage. Die Wertentwicklung in der Vergangenheit ist kein Indikator für die zukünftige Performance.